TNFSF15/TL1A:藥企巨頭搶灘布局,下一個百億級靶點(diǎn)的崛起之路
日期:2025-02-07 08:53:16
近日,關(guān)于TNFSF15/TL1A的喜報頻傳。三生國健抗TL1A單抗SSGJ-627注射液IND申請獲CDE受理,率先開啟中國藥企TL1A靶點(diǎn)臨床研究;在第43屆摩根大通年度醫(yī)療健康大會上,默沙東預(yù)估TL1A靶點(diǎn)自免治療潛力達(dá)數(shù)十億美元;梯瓦制藥也對其抗TL1A單抗duvakitug臨床數(shù)據(jù)表示滿意。
在交易市場,TL1A靶點(diǎn)也是焦點(diǎn)。2023年,默沙東以108億美元收購prometheus公司,其核心產(chǎn)品為靶向tl1a單抗; 賽諾菲與teva公司達(dá)成10億美元合作,開發(fā)teva的tl1a抗體療法tev'574; 12月,羅氏以71億美元預(yù)付款收購telavant公司,獲得rvt-3101在美國和日本的權(quán)益。2024年6月,明濟(jì)生物與艾伯維達(dá)成約17.1億美元合作,開發(fā)下一代tl1a抗體fg-m701用于治療炎癥性腸病。
TL1A靶點(diǎn)吸引眾多藥企競相布局,其背后的原因值得深入探究。作為腫瘤壞死因子超家族重要成員,TL1A在免疫調(diào)節(jié)、炎癥反應(yīng)和腫瘤發(fā)生發(fā)展等關(guān)鍵生理病理過程中扮演核心角色。下面,就讓我們從TL1A生物學(xué)特性、信號通路以及與相關(guān)疾病的關(guān)聯(lián)等方面,深入探索TL1A在藥物開發(fā)中的應(yīng)用與進(jìn)展。
1. 關(guān)于TNFSF15/TL1A
1.1 基因與蛋白結(jié)構(gòu)
TNFSF15,即腫瘤壞死因子超家族成員15,又名TL1A,為Ⅱ型跨膜蛋白,由胞內(nèi)區(qū)、跨膜區(qū)和胞外區(qū)構(gòu)成。其中,胞外區(qū)含有保守的TNF同源結(jié)構(gòu)域,這一結(jié)構(gòu)域是TNFSF15與受體結(jié)合的關(guān)鍵部位,直接決定其生物學(xué)活性 [1]。此外,胞外區(qū)還可被酶解成可溶性形式,在生物體內(nèi)發(fā)揮與膜結(jié)合形式不同的功能。
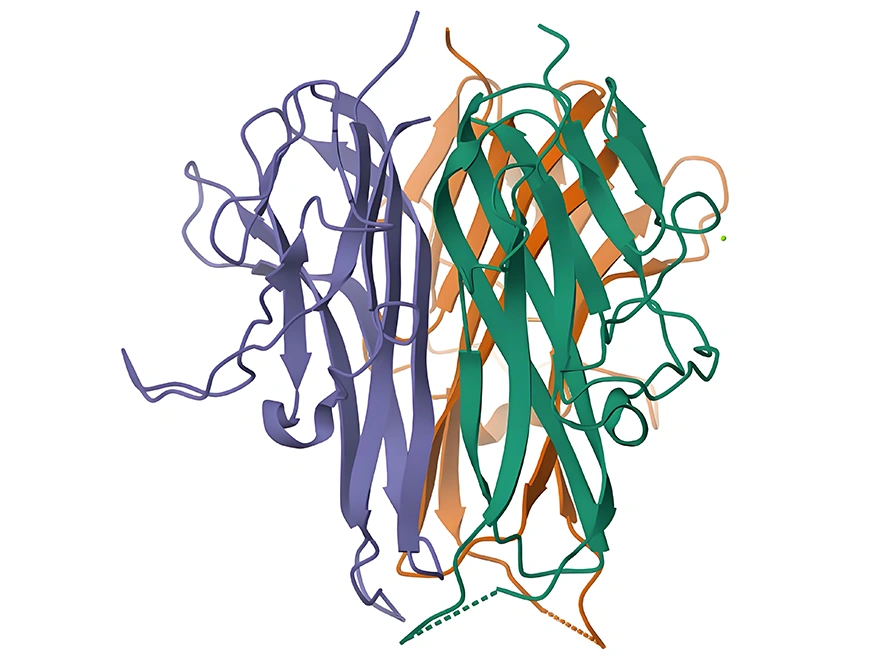
圖 1:TNFSF15 蛋白結(jié)構(gòu)示意圖
(圖源:PDB數(shù)據(jù)庫)
TNFSF15 基因由5個外顯子和4個內(nèi)含子組成。其編碼的蛋白在結(jié)構(gòu)上,胞內(nèi)區(qū)可能參與細(xì)胞內(nèi)信號的起始和調(diào)控,跨膜區(qū)負(fù)責(zé)將蛋白錨定在細(xì)胞膜上,而胞外區(qū)的TNF同源結(jié)構(gòu)域在與受體結(jié)合并激活下游信號傳導(dǎo)中起決定性作用 [1,2]。不同物種間TNFSF15基因和蛋白序列具有一定保守性,暗示其功能重要性和進(jìn)化上的保守性。
1.2 表達(dá)與調(diào)控機(jī)制
TNFSF15在多種免疫細(xì)胞,如T細(xì)胞、B細(xì)胞、單核細(xì)胞等中均有表達(dá)。其表達(dá)受多種因素精細(xì)調(diào)控,包括炎癥因子、轉(zhuǎn)錄因子等。在炎癥狀態(tài)下,TNF-α、IL-1β等炎癥因子可通過與細(xì)胞表面相應(yīng)受體結(jié)合,激活細(xì)胞內(nèi)信號通路,誘導(dǎo)TNFSF15表達(dá)上調(diào),進(jìn)而參與炎癥反應(yīng)的級聯(lián)放大 [2,3]。此外,一些轉(zhuǎn)錄因子如NF-κB等,也可直接結(jié)合到TNFSF15基因啟動子區(qū)域,調(diào)控其轉(zhuǎn)錄水平。
1.3 相關(guān)信號通路
TNFSF15主要通過與受體DR3結(jié)合來激活信號通路。二者結(jié)合后,招募銜接蛋白TRADD,進(jìn)而激活NF-κB和MAPK 等多條信號通路。NF-κB信號通路的激活可促進(jìn)一系列炎癥因子、抗凋亡蛋白等的表達(dá),影響細(xì)胞的存活、增殖和炎癥反應(yīng);而MAPK信號通路則在細(xì)胞增殖、分化和凋亡等過程中發(fā)揮重要調(diào)控作用 [2,3]。
2. TNFSF15/TL1A 與疾病的關(guān)聯(lián)
2.1 TNFSF15/TL1A與自身免疫性疾病
● 炎癥性腸病
炎癥性腸病(IBD)主要包括克羅恩病和潰瘍性結(jié)腸炎,是一類病因尚不明確的慢性非特異性腸道炎癥性疾病。大量研究表明,TNFSF15基因多態(tài)性與IBD易感性密切相關(guān) [7]。在IBD患者的腸道組織中,TNFSF15表達(dá)顯著升高。從作用機(jī)制看,TNFSF15通過其DR3受體在腸道炎癥級聯(lián)和纖維化中起關(guān)鍵作用 。它通過激活NF-κB信號通路,促使炎癥因子如IL6、IL8、TNF-α等大量釋放,引發(fā)腸道黏膜的炎癥損傷和免疫紊亂 [3,7]。臨床研究發(fā)現(xiàn),IBD患者血清和腸道黏膜中TNFSF15水平與疾病活動度呈正相關(guān),可作為評估疾病嚴(yán)重程度和預(yù)后的潛在生物標(biāo)志物。
多項(xiàng)遺傳學(xué)研究對不同種族IBD患者進(jìn)行分析,均發(fā)現(xiàn)TNFSF15基因特定單核苷酸多態(tài)性(SNP)位點(diǎn)與疾病風(fēng)險增加相關(guān) [7]。在動物實(shí)驗(yàn)中,敲除TNFSF15基因或阻斷其信號通路,可顯著減輕實(shí)驗(yàn)性結(jié)腸炎小鼠的腸道炎癥癥狀,表現(xiàn)為腸道黏膜損傷減輕、炎癥因子表達(dá)降低等。并且,使用中和TNFSF15抗體可有效逆轉(zhuǎn)結(jié)腸纖維化,使其恢復(fù)到最初的炎癥前水平,這種逆轉(zhuǎn)可能歸因于結(jié)締組織生長因子、IL31Ra、TGF-β1和IGF-1的表達(dá)減少 。
● 類風(fēng)濕關(guān)節(jié)炎
類風(fēng)濕關(guān)節(jié)炎是一種以關(guān)節(jié)滑膜炎癥為主要特征的自身免疫性疾病,可導(dǎo)致關(guān)節(jié)疼痛、腫脹、畸形,嚴(yán)重影響患者生活質(zhì)量。在類風(fēng)濕關(guān)節(jié)炎患者體內(nèi),TNFSF15 水平明顯升高 [4]。其可刺激滑膜細(xì)胞增殖,促進(jìn)炎癥因子如 IL-1、IL-6、TNF-α等的分泌,這些炎癥因子進(jìn)一步激活免疫細(xì)胞,形成炎癥惡性循環(huán),導(dǎo)致關(guān)節(jié)軟骨和骨質(zhì)破壞 [4]。研究還發(fā)現(xiàn),TNFSF15可通過誘導(dǎo)破骨細(xì)胞分化和活化,加速關(guān)節(jié)骨質(zhì)吸收,加重關(guān)節(jié)損傷。臨床研究表明,類風(fēng)濕關(guān)節(jié)炎患者血清TNFSF15水平與疾病活動指數(shù)、關(guān)節(jié)破壞程度相關(guān) [4]。
2.2 TNFSF15/TL1A與腫瘤
● 對腫瘤血管生成的影響
腫瘤的生長和轉(zhuǎn)移依賴于充足的血液供應(yīng),血管生成在這一過程中起著關(guān)鍵作用。TNFSF15可通過調(diào)節(jié)血管內(nèi)皮生長因子(VEGF)等血管生成因子的表達(dá),促進(jìn)腫瘤血管生成 [5,8]。研究發(fā)現(xiàn),TNFSF15可激活腫瘤細(xì)胞或腫瘤微環(huán)境中的相關(guān)信號通路,上調(diào)VEGF的表達(dá)和分泌 [5,8]。VEGF與其受體結(jié)合后,可促進(jìn)血管內(nèi)皮細(xì)胞的增殖、遷移和管腔形成,為腫瘤生長和轉(zhuǎn)移提供營養(yǎng)支持。在多種實(shí)體腫瘤如乳腺癌、肺癌、結(jié)直腸癌中,均觀察到TNFSF15與腫瘤血管生成的密切關(guān)聯(lián)。
臨床研究表明,腫瘤組織中TNFSF15表達(dá)水平與腫瘤微血管密度呈正相關(guān),高表達(dá)TNFSF15的腫瘤患者往往預(yù)后較差 [8]。在動物實(shí)驗(yàn)中,抑制TNFSF15的功能可顯著減少腫瘤血管生成,抑制腫瘤生長和轉(zhuǎn)移。
● 與腫瘤免疫微環(huán)境
腫瘤免疫微環(huán)境是腫瘤細(xì)胞與免疫細(xì)胞、間質(zhì)細(xì)胞及細(xì)胞外基質(zhì)等共同構(gòu)成的復(fù)雜生態(tài)系統(tǒng)。TNFSF15在腫瘤免疫微環(huán)境中發(fā)揮著雙重調(diào)節(jié)作用 [6]。一方面,TNFSF15可激活T細(xì)胞和NK細(xì)胞,增強(qiáng)機(jī)體的抗腫瘤免疫反應(yīng) [6]。它可促進(jìn)T細(xì)胞的增殖、分化和細(xì)胞因子分泌,增強(qiáng)T細(xì)胞對腫瘤細(xì)胞的殺傷活性;同時,也可激活NK細(xì)胞,使其發(fā)揮更強(qiáng)的細(xì)胞毒性作用。另一方面,在某些腫瘤微環(huán)境中,TNFSF15可誘導(dǎo)免疫抑制細(xì)胞如調(diào)節(jié)性T細(xì)胞(Treg)和髓源性抑制細(xì)胞(MDSC)的產(chǎn)生和聚集,促進(jìn)腫瘤免疫逃逸。
臨床研究發(fā)現(xiàn),在部分腫瘤患者中,腫瘤組織中TNFSF15的表達(dá)水平與Treg細(xì)胞浸潤呈正相關(guān),與腫瘤患者的不良預(yù)后相關(guān) [6]。而在另一些腫瘤中,高表達(dá)的TNFSF15則與較好的免疫浸潤和預(yù)后相關(guān) [6]。這提示TNFSF15在腫瘤免疫微環(huán)境中的作用可能因腫瘤類型、分期和個體差異而有所不同。
3. TNFSF15/TL1A 相關(guān)藥物研發(fā)進(jìn)展
目前,已有多款靶向TNFSF15的抗體藥物進(jìn)入臨床試驗(yàn)階段。這些抗體藥物主要通過特異性地結(jié)合TNFSF15,阻斷其與受體DR3的相互作用,從而抑制下游信號傳導(dǎo),達(dá)到治療疾病的目的。主要適應(yīng)癥為潰瘍性結(jié)腸炎、克羅恩病等,最高研究階段臨床3期。部分整理如下表:
| 藥物 | 藥物類型 | 在研適應(yīng)癥 | 在研機(jī)構(gòu) | 最高研發(fā)階段 |
|---|---|---|---|---|
| Afimkibart | 單克隆抗體 | 活動性中度潰瘍性結(jié)腸炎 | 活動性重度潰瘍性結(jié)腸炎 | 潰瘍性結(jié)腸炎 | 克羅恩病 | Hoffmann-La Roche, Inc. | F. Hoffmann-La Roche Ltd. | Hoffmann-La Roche Ltd. | Roivant Sciences Ltd. | Roche Holding AG | 臨床3期 |
| Tulisokibart | 單克隆抗體 | 克羅恩病 | 潰瘍性結(jié)腸炎 | 彌漫性硬皮病 | 系統(tǒng)性硬化相關(guān)的間質(zhì)性肺病 | 活動性中度潰瘍性結(jié)腸炎 | 活動性重度潰瘍性結(jié)腸炎 | Prometheus Biosciences, Inc. | Merck Sharp & Dohme Corp. | Merck Sharp & Dohme LLC | 默沙東研發(fā)(中國)有限公司 | 臨床3期 |
| Duvakitug | 單克隆抗體 | 潰瘍性結(jié)腸炎 | 克羅恩病 | Sanofi | Teva Branded Pharmaceutical Products R&D, Inc. | 臨床2期 |
| XmAb942(Xencor) | 單克隆抗體 | 潰瘍性結(jié)腸炎 | Xencor, Inc. | 臨床1/2期 |
| BCD-261 | 單克隆抗體 | - | Biocad CJSC | 臨床1期 |
| PF-07261271 | 雙特異性抗體 | 炎癥性腸病 | Pfizer Inc. | 臨床1期 |
| SPY-002 | 單克隆抗體 | 炎癥性腸病 | Spyre Therapeutics, Inc. | 臨床1期 |
| SSGJ-627 | 單克隆抗體 | - | 三生國健藥業(yè)(上海)股份有限公司 | 臨床申請 |
在自身免疫性疾病方面,初步臨床試驗(yàn)結(jié)果顯示,這些靶向TNFSF15的抗體藥物具有較好的療效和安全性。例如,在炎癥性腸病的臨床試驗(yàn)中,使用這些抗體藥物治療后,患者的腸道炎癥癥狀得到明顯改善,疾病活動度降低,且不良反應(yīng)輕微。
在腫瘤治療領(lǐng)域,雖然靶向TNFSF15的抗體藥物仍處于探索階段,但已有研究表明,其與其他抗腫瘤治療方法如化療、免疫治療聯(lián)合使用,可增強(qiáng)抗腫瘤效果 [1,2]。
4. TNFSF15/TL1A研究相關(guān)產(chǎn)品推薦
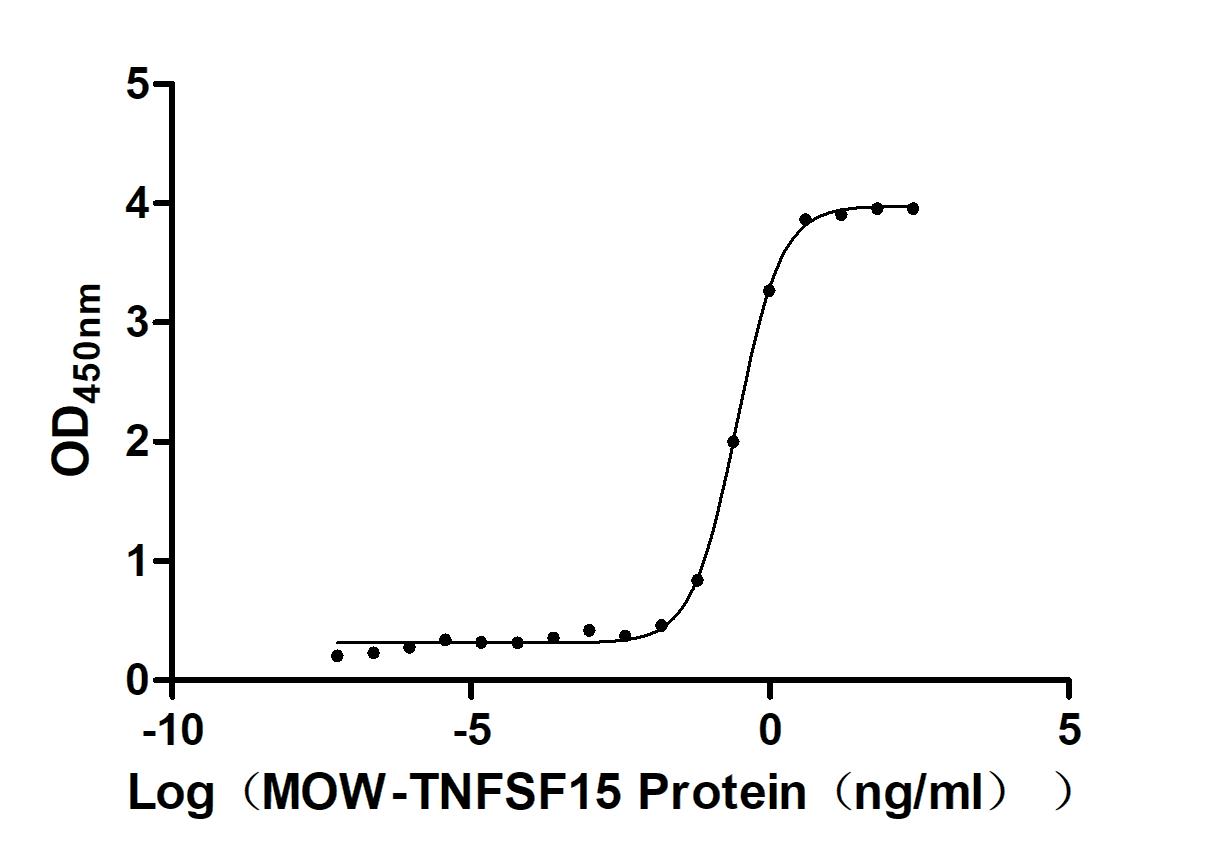
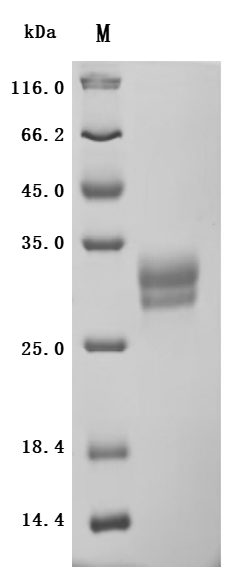
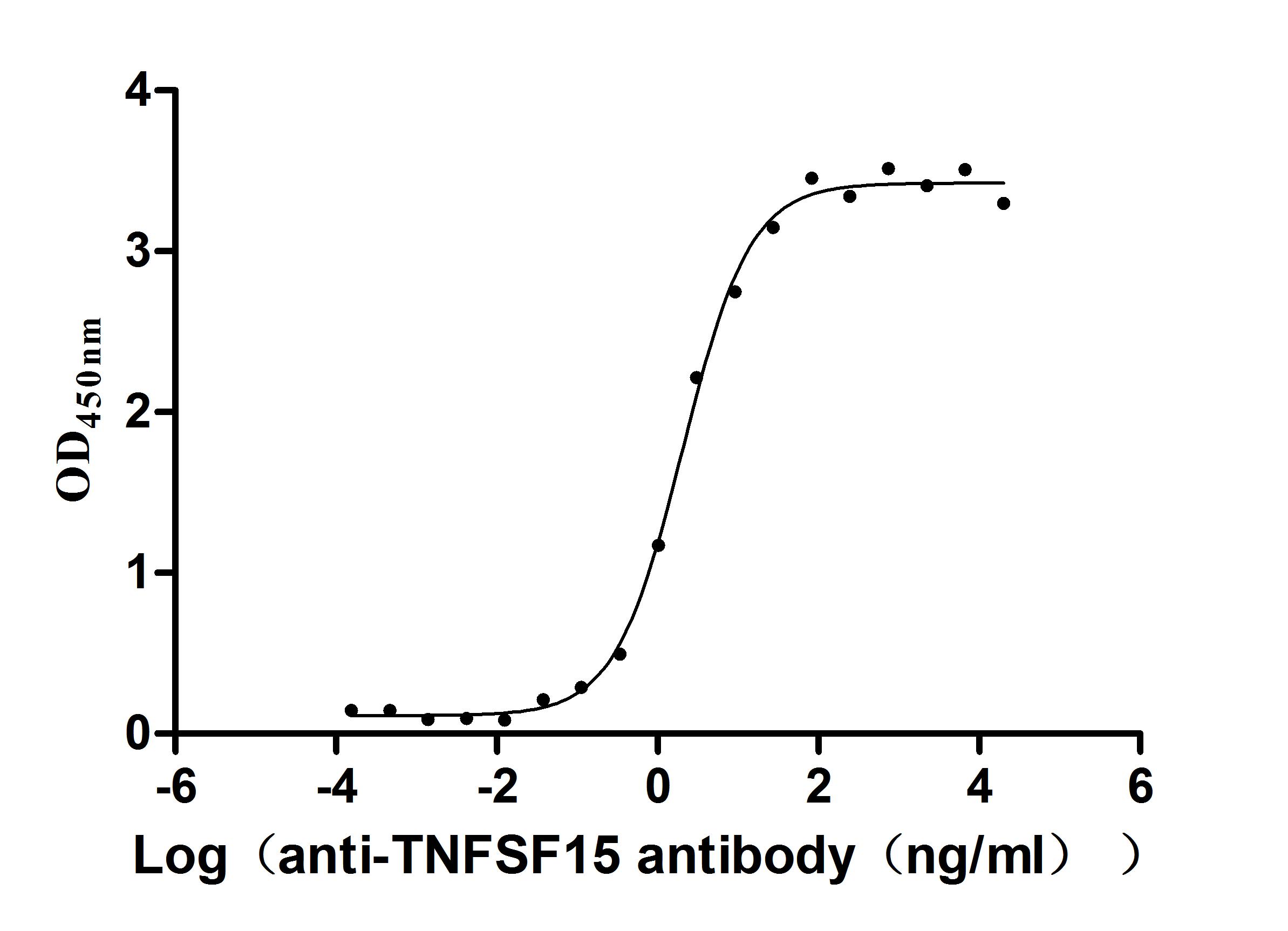
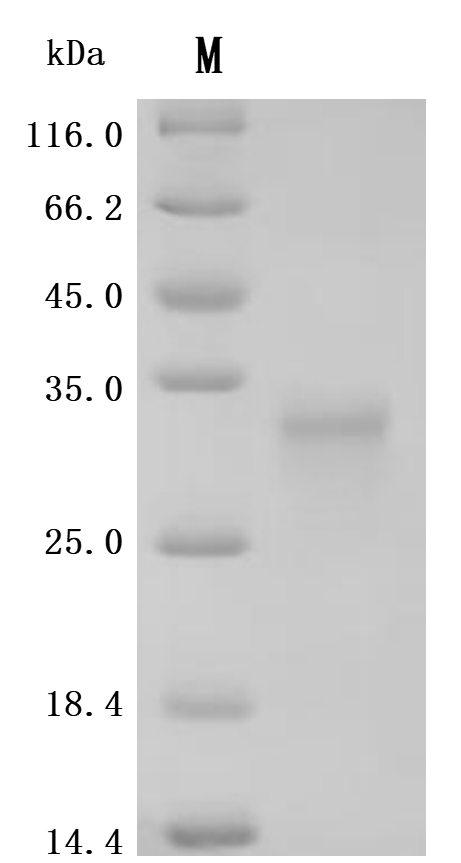
為助力各藥企及科研機(jī)構(gòu)研發(fā)人員對TNFSF15/TL1A 的研究,華美生物重磅推出多款高活性的TNFSF15/TL1A蛋白產(chǎn)品,覆蓋人、小鼠、猴等多種屬,并提供TNFSF15/TL1A 抗體及ELISA試劑盒產(chǎn)品,助力您在TNFSF15/TL1A機(jī)制方面的研究或其潛在臨床價值的探索。
● TNFSF15/TL1A 重組蛋白
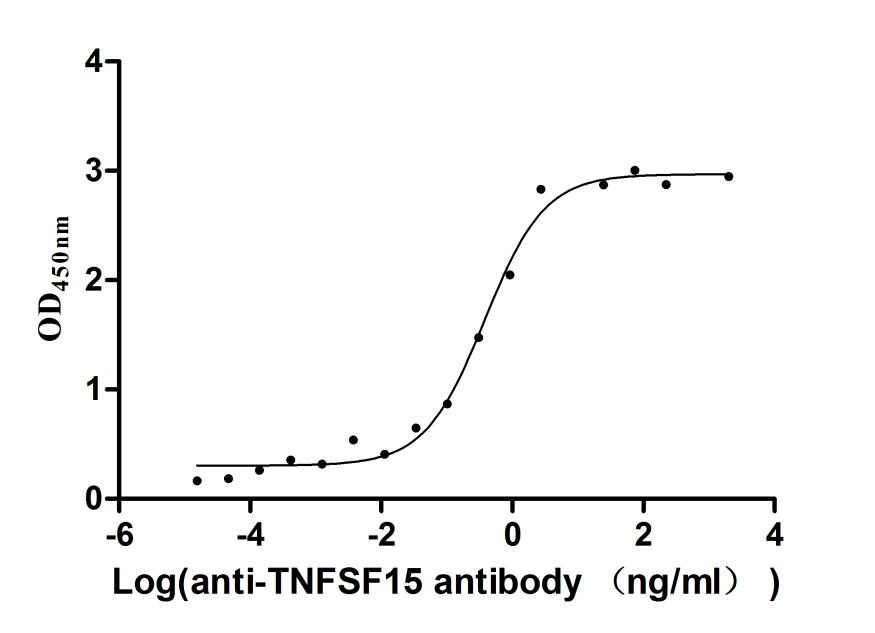
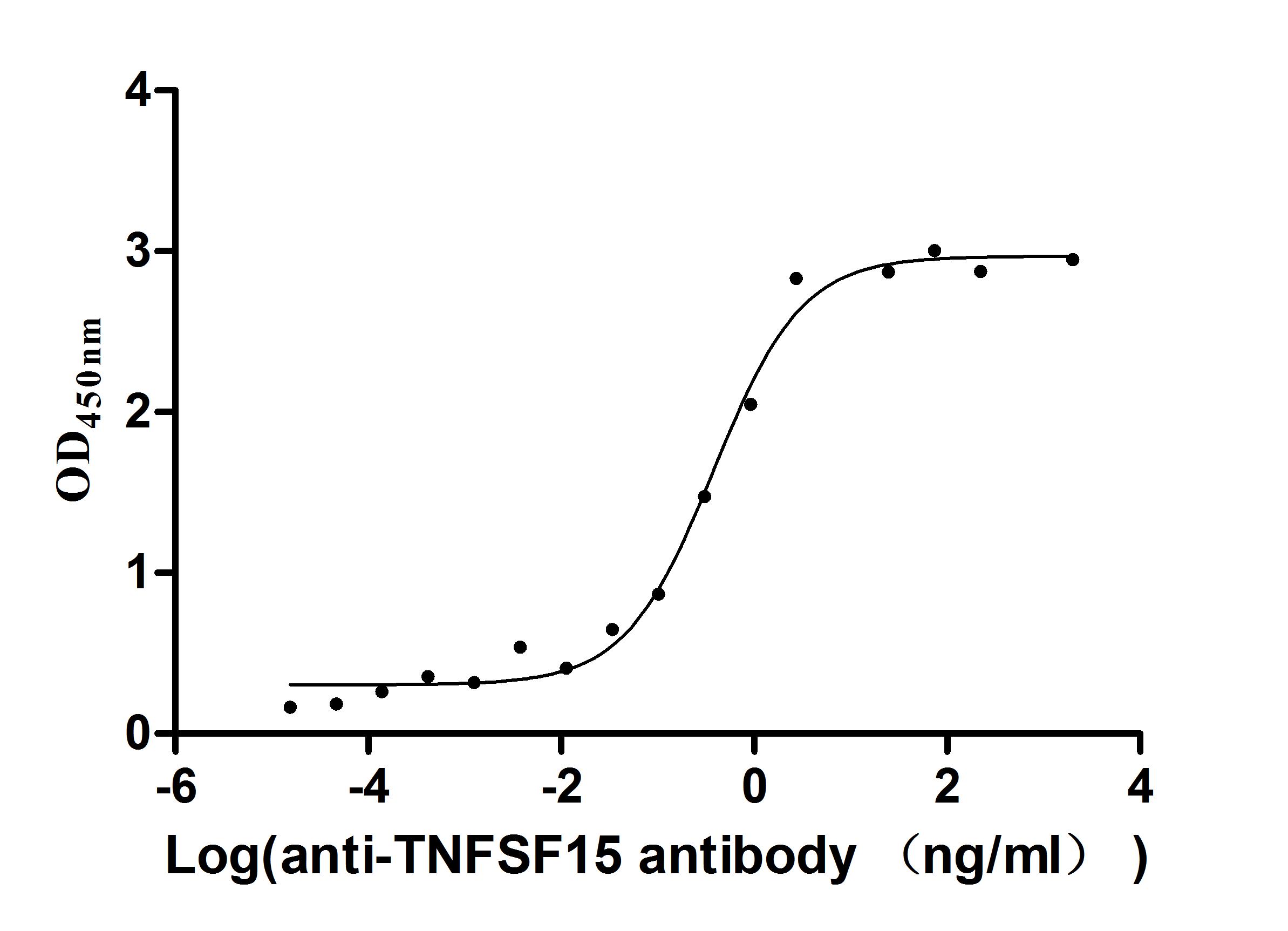
● TNFSF15/TL1A 抗體
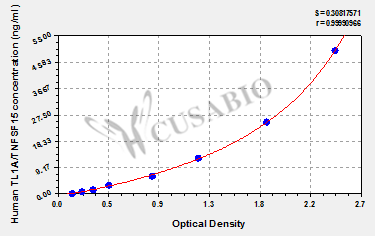
● TNFSF15/TL1A 酶免試劑盒
點(diǎn)擊查看TNFSF15/TL1A所有相關(guān)產(chǎn)品
參考文獻(xiàn):
[1] Smith CA, Farrah T, Goodwin RG. The TNF receptor superfamily of cellular and viral proteins: activation, costimulation, and death. Cell. 1994;76(6):959 - 962.
[2] Aggarwal BB. Signaling pathways of the TNF - superfamily: a double - edged sword. Nat Rev Immunol. 2003;3(9):745 - 756.
[3] Neurath MF. TNFalpha in inflammatory bowel disease: friend or foe? Trends Mol Med. 2003;9(11):518 - 524.
[4] Chabaud M, Fossiez F, Taupin JL, et al. Overexpression of interleukin - 15 in rheumatoid synovium and in interleukin - 1 - stimulated rheumatoid synovial fibroblasts. Arthritis Rheum. 1996;39(4):681 - 689.
[5] Ferrara N, Gerber HP, LeCouter J. The biology of VEGF and its receptors. Nat Med. 2003;9(6):669 - 676.
[6] Dunn GP, Bruce AT, Ikeda H, Old LJ, Schreiber RD. Cancer immunoediting: from immunosurveillance to tumor escape. Nat Immunol. 2002;3(11):991 - 998.
[7] Zhang X, Li Y, Wang Y, et al. TNFSF15 polymorphisms and susceptibility to inflammatory bowel disease: a meta - analysis. Inflamm Bowel Dis. 2012;18(10):1864 - 1873.
[8] Yang Z, Wang Y, Li Y, et al. TNFSF15 promotes angiogenesis in colorectal cancer by upregulating VEGF expression. Oncol Rep. 2015;33(2):671 - 673.


-AC1.jpg)
-SDS.jpg)