神經科學研究最新前沿進展
日期:2018-10-26 11:41:46

神經系統是機體內對生理功能活動的調節起主導作用的系統,本次整理多篇神經科學相關研究成果,助科研朋友們共同探索神經學的奧秘!
【1】Cell:人類神經元為何如此獨特?
在一項新的研究中,來自美國麻省理工學院、麻省總醫院和哈佛醫學院的研究人員證實不同于其他動物的神經元,人神經元使用高度分隔的信號。人神經元的樹突處理電信號的方式與嚙齒類動物不同。
Harnett說,“人們長期使用動物模型來研究癲癇,但是很明顯的是,至少在神經元的樹突中,人類和嚙齒類動物之間存在一些非常顯著的差異。我們越了解離子通道和膜興奮性,我們就越能深入了解癲癇的發病機制以及如何治療它。”這項研究最終可能也有益于癲癇患者。
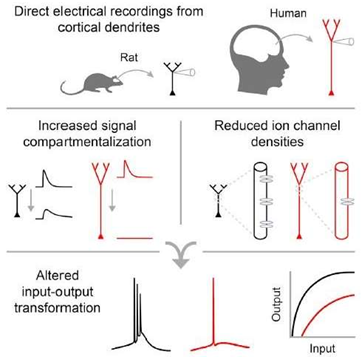
圖片來源Cell
>>>EnhancedDendritic Compartmentalization in Human Cortical Neurons.
doi:10.1016/j.cell.2018.08.045.
【2】Science:發現神經嵴細胞遷移有望修復面部缺陷
在一項新的研究中,來自英國和西班牙的研究人員發現形成面部特征的胚胎干細胞,稱為神經嵴細胞(neural crest cell),使用一種意想不到的機制,從頭部后面移動到前面,從而定植在面部中。這一發現可能有助于了解面部缺陷是如何形成的,從而讓人們更接近一步修復胚胎中的顱面畸形(craniofacial malformation)。這種新的機制可能在其他的涉及細胞運動的過程中起著重要的作用。
>>>Supracellularcontraction at the rear of neural crest cell groups drives collectivechemotaxis.
doi:10.1126/science.aau3301.
【3】PNAS:研究揭示FUS誘導神經退行性疾病的新機制
《美國國家科學院院刊》(PNAS)近期報道了RNA結合蛋白FUS與線粒體ATP合成酶beta亞基相互作用并誘導線粒體去折疊蛋白反應(UPRmt)的新機制。這一研究為核定位的RNA結合蛋白靶向線粒體ATP合成酶提供了首要證據,為未來開發治療衰老相關神經退行性疾病的診斷工具和治療方法提供重要研究思路。
在本文的研究中,研究人員利用FUS蛋白病的可誘導細胞模型進行實驗,證明FUS表達引起的線粒體功能缺陷是發生在細胞死亡之前的早期變化。FUS靶向線粒體ATP合成從而激活UPRmt的研究結果,揭示了FUS誘導神經退行性疾病的新機制,提示線粒體損傷可能是FTLD-FUS和ALS-FUS等多種神經退行性疾病的共有機制,阻斷線粒體損傷可能有助于治療這些毀滅性疾病。
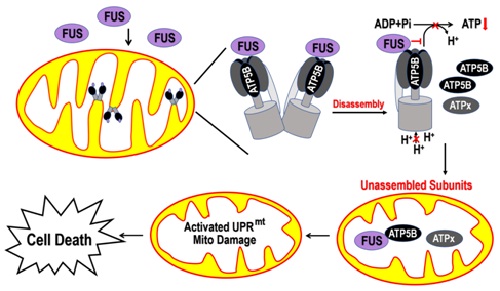
FUS誘導線粒體損傷和神經毒性的分子機制模式圖
>>>FUS interacts with ATP synthase beta subunit and induces mitochondrial unfoldedprotein response in cellular and animal models.
doi:https://doi.org/10.1073/pnas.1806655115.
【4】Neuron:研究發現PDGFRβ細胞介導外周感染信號向中樞神經系統快速傳遞機制
中國科學院神經科學研究所、腦科學與智能技術卓越創新中心、神經科學國家重點實驗室于翔研究組在《神經元》期刊在線發表了題為《PDGFRβ細胞通過趨化因子CCL2介導了外周感染信號向中樞神經系統的快速傳遞》的研究性論文。
該研究發現,在系統性感染早期,小鼠腦內的PDGFRβ細胞快速感應循環系統中的感染信號,并通過釋放趨化因子CCL2增強多個腦區神經元的興奮性突觸傳遞與放電頻率。PDGFRβ細胞是一種血管旁細胞,是大腦神經血管單元與血腦屏障的重要組成部分,具有維持血腦屏障、調控血管血流量等功能。
>>>PDGFRβCells Rapidly Relay Inflammatory Signal from the Circulatory System to Neuronsvia Chemokine CCL2
doi:https://doi.org/10.1016/j.neuron.2018.08.030
【5】Science:將人腦細胞移植到小鼠大腦中有助深入認識唐氏綜合癥等神經疾病
來自英國、葡萄牙和瑞士的研究人員將人腦細胞移植到小鼠大腦中,首次觀察到它們如何生長和彼此之間建立連接。這允許他們在一種比以前更自然的環境中研究人腦細胞之間相互作用的方式。
基于這種技術,他們通過使用由兩名唐氏綜合癥患者捐獻的細胞構建出唐氏綜合癥模型。此外,他們還描述了來自唐氏綜合癥患者的腦細胞與來自沒有患上這種疾病的人的腦細胞之間的差異。他們表示,他們的方法可能在未來用于研究一系列腦部疾病,包括精神分裂癥,癡呆癥和自閉癥。
在這項新的研究中,這些研究人員采用了一種革命性的稱為體內雙光子顯微鏡(in vivo 2-photon microscopy)的技術,這允許他們不僅能夠觀察單個活的腦細胞,而且也能夠觀察它們之間形成的連接。
>>>Invivo modeling of human neuron dynamics and Down syndrome.
doi:10.1126/science.aau1810.
【6】Neuroscience Bulletin:研究揭示跨期決策的神經網絡具有獲得-損失不對稱性
近年來,神經科學領域越來越傾向于通過考察多個腦區之間的功能交互來理解人們的復雜認知功能。其中兩個常用方法是心理生理交互(psychophysiological interaction, PPI)分析及動態因果模型(dynamic causal modeling, DCM)。PPI分析可以衡量任務如何調控一個腦區對另一腦區的影響;DCM分析則可以同時確定網絡中腦區之間的因果關系,以及任務對腦區間效應連接的調節作用。
研究結果表明,跨期決策在獲得和損失領域中涉及了不同的評價腦區和動態交互網絡。該研究為理解獲得-損失領域下跨期決策的神經機制提供了一個新的生物學視角。
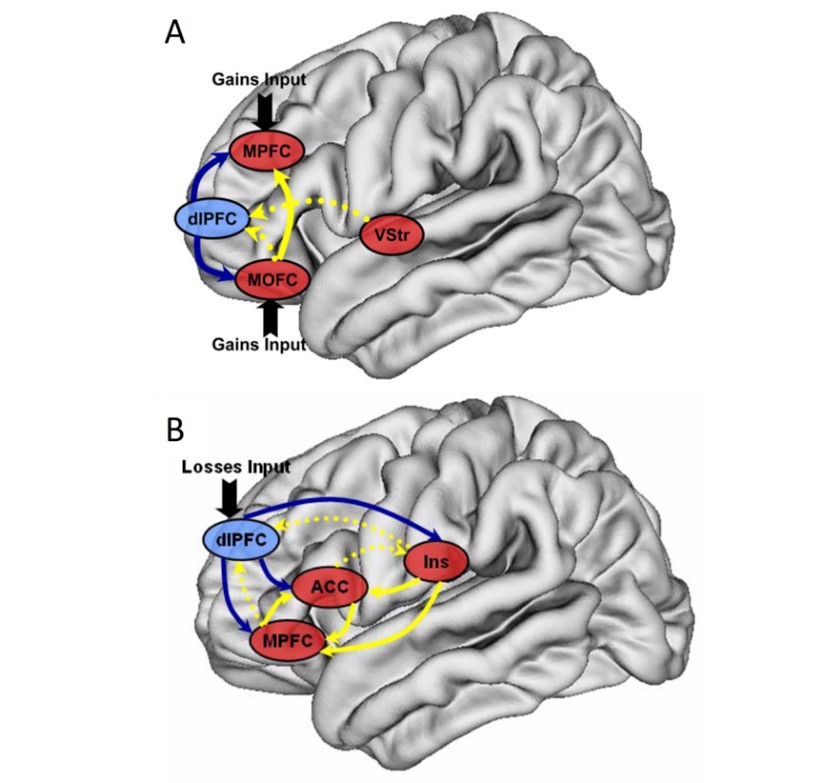
獲得(A)和損失(B)跨期決策任務中的最優動態因果模型
>>>Separate Neural Networks for Gains and Losses inIntertemporal Choice.
doi:https://doi.org/10.1007/s12264-018-0267-x
【7】Science:重磅!發現重寫創傷記憶的神經元
對創傷經歷的回憶會導致精神健康問題,如創傷后應激障礙(PTSD),這會破壞一個人的生活。據估計,當前將近三分之一的人會在他們生命中的某個時刻遭受恐懼或應激相關的障礙。如今,一項新的研究在細胞水平展示了一種療法如何能夠治療長期的創傷記憶。
在治療創傷記憶領域,對恐懼衰減(fearattenuation)是否涉及通過新的安全記憶痕跡(memory trace of safety)或將原始的恐懼記憶痕跡(memory trace of fear)重寫為安全記憶痕跡來抑制原始的恐懼記憶痕跡,人們長期以來爭論不止。
這種爭論的一部分與我們總體上還不能完全理解神經元如何存儲記憶的事實相關。雖然這項研究取得的新發現不能排除這種抑制機制,但是它們首次證實了重寫創傷記憶在治療創傷記憶中的重要性。
>>>Reactivationof recall-induced neurons contributes to remote fear memory attenuation.
doi:10.1126/science.aas9875
【8】Cell Reports:藍斑去甲腎上腺- 素神經系統在全身麻醉中的重要作用
為了研究藍斑去甲腎上腺*素系統在靜脈全身麻醉中的作用機制,研究人員通過檢測靜脈全身麻醉藥丙泊酚(propofol)和依托咪酯(etomidate)引起的運動水平、大腦局部場電位活動和外周運動神經元活動的變化,首次建立了完善的斑馬魚靜脈全身麻醉模型。
該研究以斑馬魚為模式動物,發現臨床最常用的兩種靜脈麻醉藥丙泊酚和依托咪酯,通過抑制藍斑去甲腎上腺-素能神經元突觸前興奮性輸入及其本身的興奮性,從而影響麻醉的誘導和蘇醒過程。該工作揭示了藍斑神經系統對全身麻醉狀態起到重要的調節作用。
>>>TheLocus Coeruleus Modulates Intravenous General Anesthesia of Zebrafish via aCooperative Mechanism.
doi:https://doi.org/10.1016/j.celrep.2018.08.046
作生命科學的一個分支學科,神經生物學是比較特殊的,從細胞結構、信號傳導到神經疾病三個方面來研究神經系統,是生命科學的根基。人類的求知欲需要神經生物學的進步,人類的發展同樣需要神經生物學的進步。
目前神經生物學領域正處于高速發展階段,華美CUSABIO助力您的神經生物學科研!
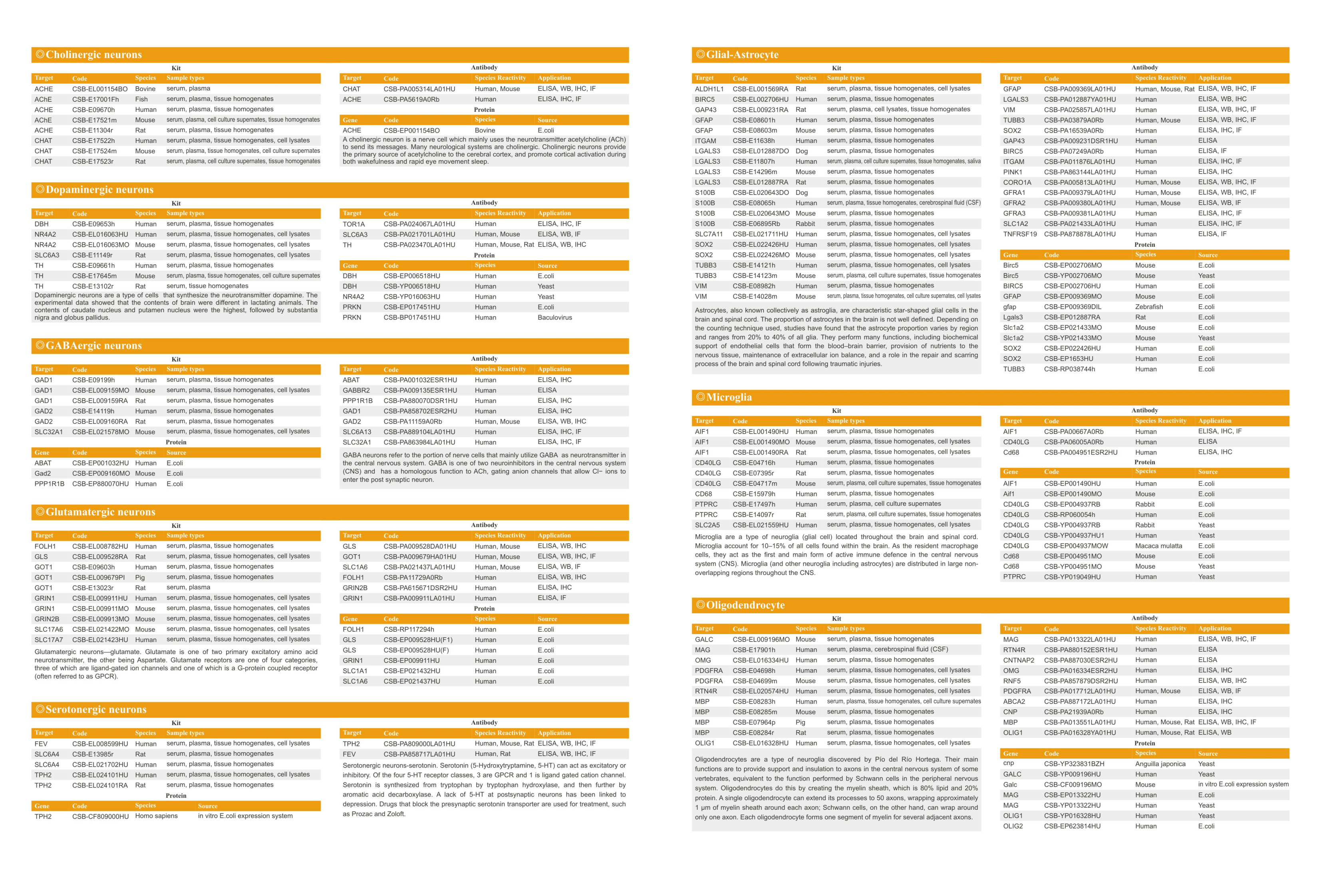
【神經學標志物相關產品——輕觸圖片查看】
后臺回復【Nerve】免費索取PDF文件
>>點擊查看相關產品詳情
↓神經學研究精品抗體2支免費試用↓
· 免費申領→ 20ug ·
微信公眾號點擊菜單欄超燃活動——試用中心
或加客服QQ2048334277 咨詢免費申領試用裝
>>NES Monoclonal Antibody
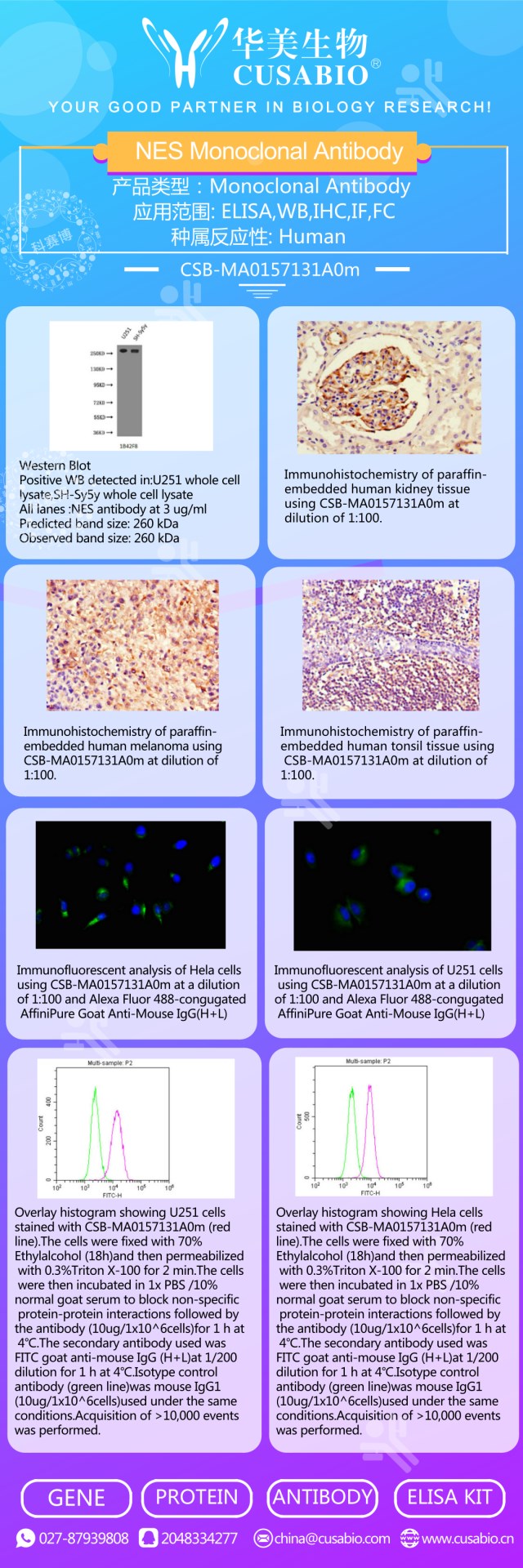
>>GFAP Monoclonal Antibody
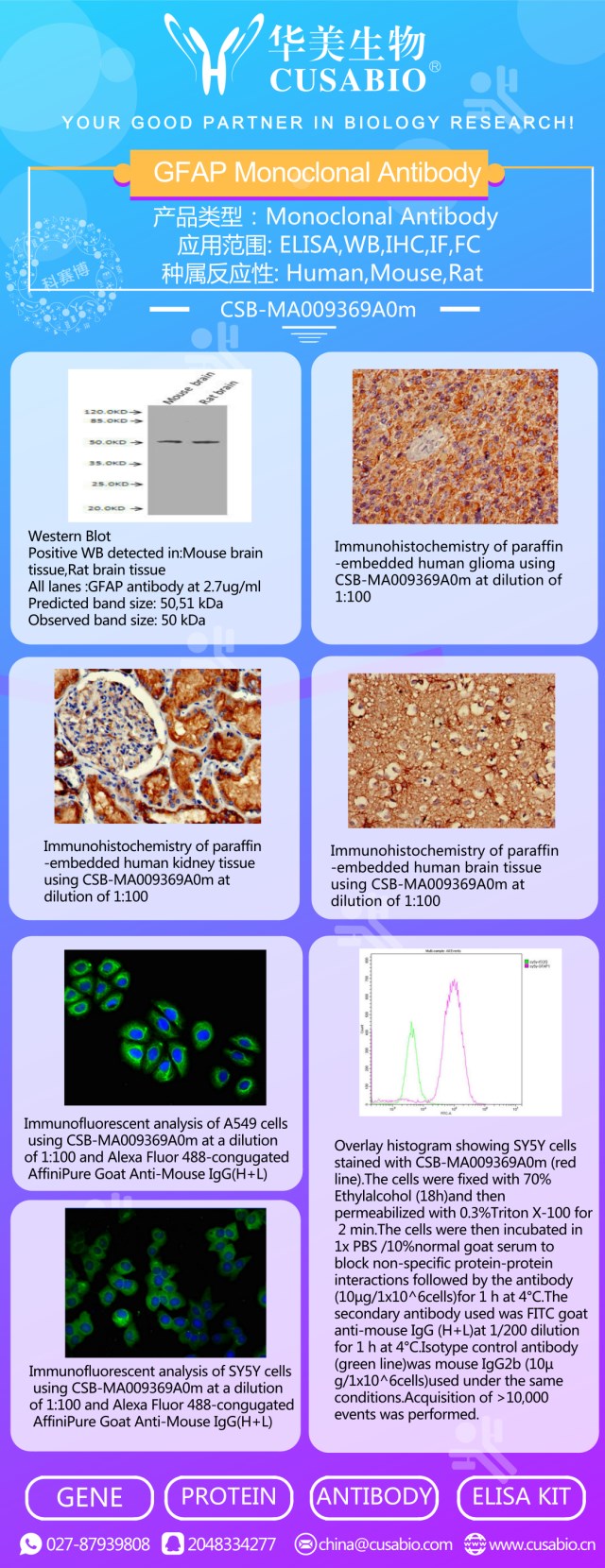
↓華美生物邀您參與美國國際神經科學協會年會展↓

匯總|神經學相關研究標志物
十月聚焦神經學研究—神經性相關疾病!
>>Do You Really Known Neurons and Glia Cells in Nerve System?

上一篇: 十月聚焦神經學研究!










