Nature | IF=69.504!抗內源性逆轉錄病毒抗體促進肺癌免疫治療
瀏覽次數:753 日期:2023-05-05 10:32:25
內源性逆轉錄病毒(endogenous retroviruses,ERV)是哺乳動物基因組的一部分,它們是逆轉錄病毒(retroviruses)在進化過程中整合進基因組的遺跡,在基因組中占據相當大的比例,但多數ERV已經失去了活性。然而,某些情況下,這些ERV可能會重新激活,進而影響基因表達和細胞功能。
肺癌是全球最常見的癌癥之一,也是最常導致死亡的癌癥。近年來,免疫治療已經成為肺癌治療的一個重要手段。弗朗西斯·克里克研究所(The Francis Crick Institute)Julian Downward和George Kassiotis等人于2023年4月發表在Nature上的一篇文章,探討了肺腺癌患者和小鼠肺腺癌引起的局部生發中心反應和腫瘤結合抗體,并進一步確定內源性逆轉錄病毒(ERV)包膜糖蛋白是主要的抗腫瘤抗體靶點。
B cell responses in a new LUAD model
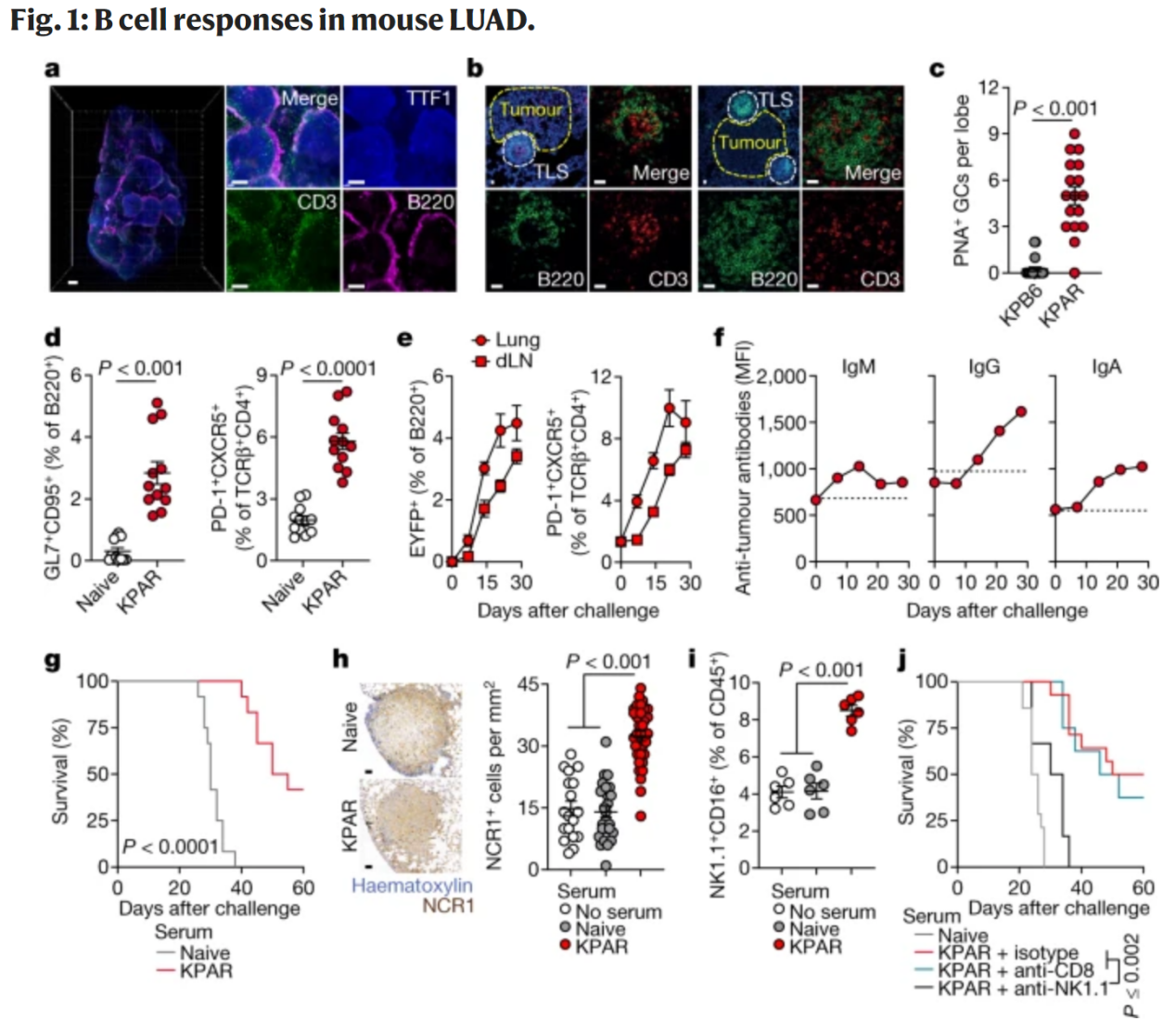
為了研究B細胞和TLS在腫瘤進展和治療反應中的作用。研究者使用了一個新建立的LUAD模型,該模型基于KPAR細胞。研究發現KPAR腫瘤能夠刺激TLS形成和生發中心反應,而KPB6腫瘤則不能。此外,KPAR受試小鼠的血清中含有與KPAR結合的抗體,具有抗腫瘤活性。將KPAR受試小鼠的血清轉移到第二批KPAR受試小鼠中,可以顯著延長受試小鼠的生存期。這些抗腫瘤活性與腫瘤浸潤的自然殺傷(NK)細胞數量的顯著增加有關。總之,這些結果表明KPAR腫瘤能誘導招募和激活B細胞,并產生具有強大抗腫瘤活性的抗體。
Anti-tumour antibodies target an ERV
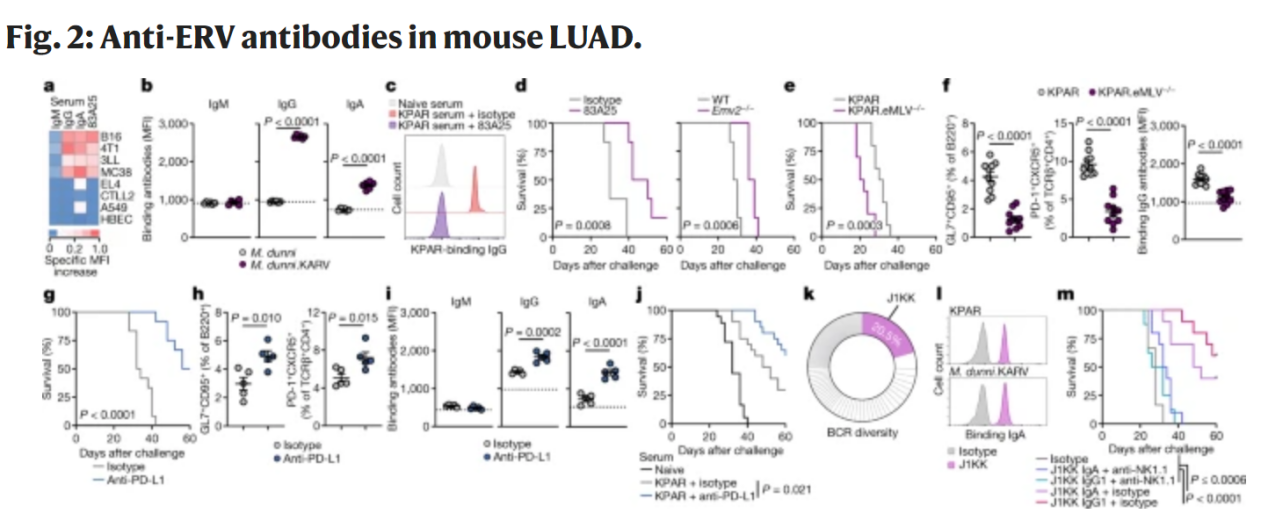
研究人員通過實驗探究KPAR模型中抗腫瘤抗體特異性的過程,發現抗腫瘤抗體在KPAR模型中主要靶向一類異常表達的內源性逆轉錄病毒(ERV),這可能為腫瘤免疫治療提供了新的靶點。在KPAR腫瘤模型中,研究人員發現了一種具有感染性的KPAR相關逆轉錄病毒(KARV),并證明其是主要的抗體靶點。通過使用83A25治療,研究人員觀察到野生型小鼠對KPAR挑戰的生存期顯著延長,同時在缺乏eMLV包膜糖蛋白免疫耐受的Emv2缺陷小鼠中,KPAR腫瘤生長受到延遲。這些發現揭示了異常表達的ERV作為自發產生的針對KPAR腫瘤的保護性抗腫瘤抗體的主要靶點,為未來腫瘤免疫治療研究提供了新的方向。
PD-L1 blockade boosts anti-ERV response
在本文中,研究者還探討了抗腫瘤抗體和GC反應是否對PD-1或PD-L1阻斷的治療效果有貢獻。實驗發現,PD-L1阻斷顯著延長了KPAR腫瘤小鼠的生存期,并擴大了局部GC B細胞和TFH細胞反應。PD-L1阻斷還顯著提高了腫瘤結合IgG和IgA抗體的滴度。此外,來自PD-L1阻斷治療小鼠的血清中,IgG和IgA抗體對KARV(KPAR相關逆轉錄病毒)感染的M. dunni細胞的結合增加,說明抗ERV抗體對KPAR腫瘤排斥的未處理和ICB治療有貢獻。總之,這些數據表明,抗PD-L1治療增強了對特定ERV抗原的抗體反應,并提高了抗腫瘤抗體的功能,從而改善了腫瘤治療效果。
B cell responses in targeted therapies
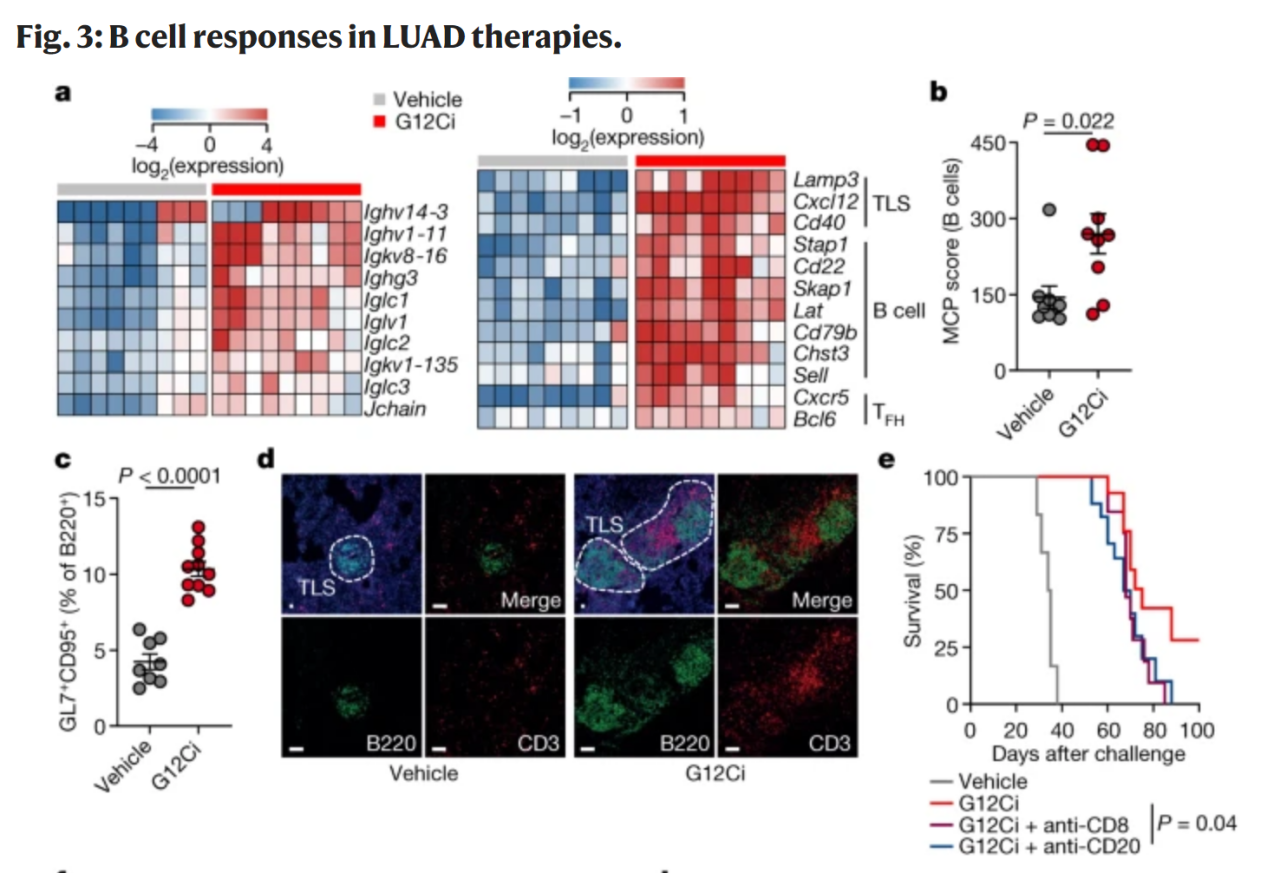
為了探討抗腫瘤B細胞反應是否對除ICB外的其他治療方法產生治療效果。研究者使用了靶向治療方法,包括高度選擇性的KRAS(G12C)抑制劑(G12Ci)。研究表明,針對性治療KRAS(G12C)抑制劑G12Ci可促進抗腫瘤B細胞反應,而全身性抑制MEK會阻礙這些反應。在G12Ci治療的小鼠模型中,B細胞可能對持久抗腫瘤反應和免疫記憶有積極作用。這些發現有助于了解B細胞在腫瘤治療中的作用,并指導未來的免疫治療策略。
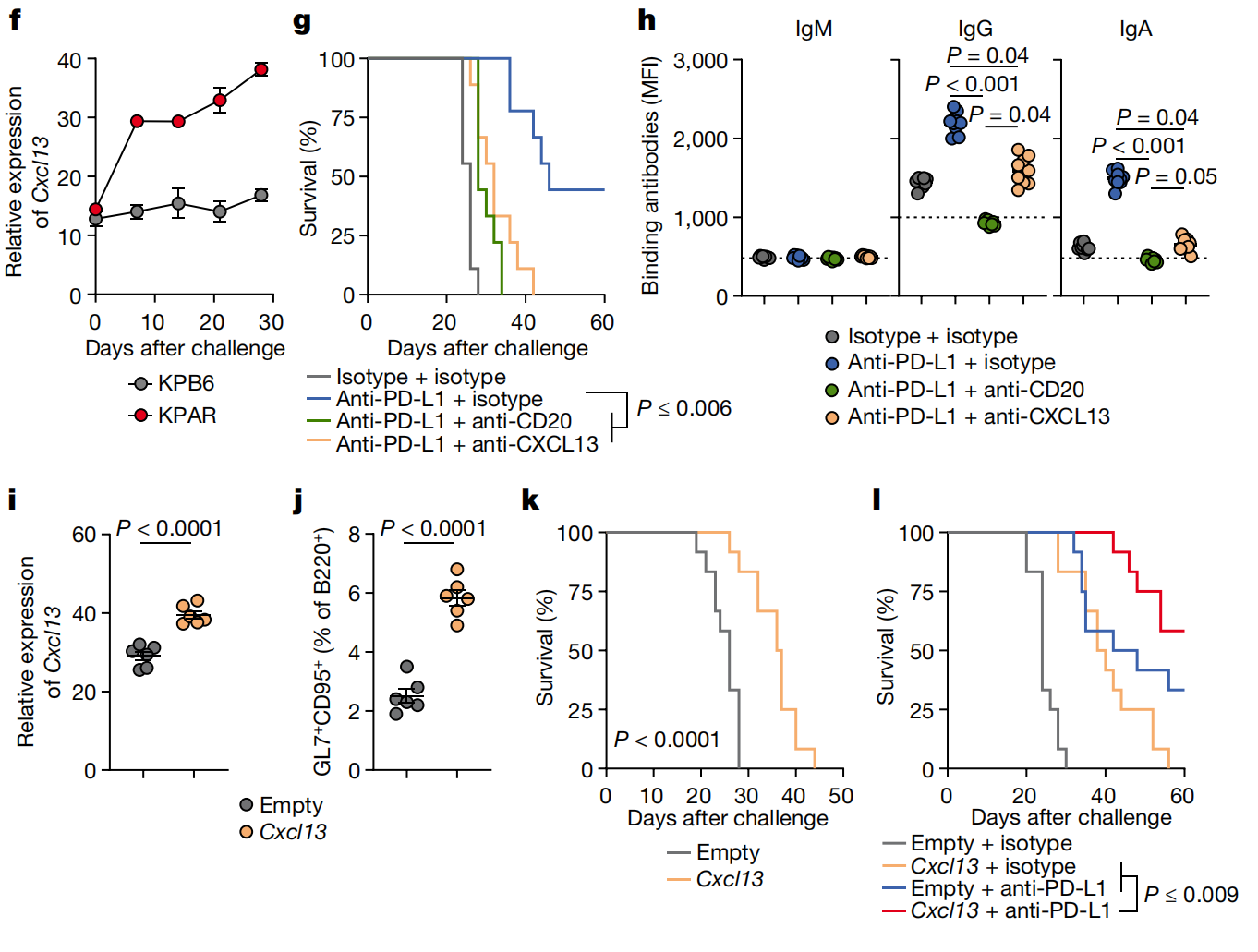
這部分研究探討了CXCL13治療與免疫檢查點抑制劑(ICB)的協同作用。研究發現抑制淋巴結結構組織化趨化因子CXCL13會減弱抗PD-L1治療的肺部GC B細胞反應并抵消ICB的治療效果。為了檢驗CXCL13的治療效果,研究者通過鼻內給藥法增加了腫瘤負荷肺部的Cxcl13表達。結果發現,這種治療增加了GC B細胞反應并顯著延長了小鼠的生存期。更進一步,將CXCL13和抗PD-L1治療結合使用比單獨使用任一治療方法能進一步延長生存期,突顯了吸入式免疫調節與ICB協同作用的潛力。
這項研究探討了肺腺癌(LUAD)患者中B細胞反應的作用。研究者發現LUAD和肺鱗狀細胞癌(LUSC)腫瘤區域的B細胞特征和TLS轉錄特征與正常肺組織相比有所變化。LUAD患者中的B細胞標記物(如CD79A、CD19和MS4A1)的高表達與更好的預后相關,而在LUSC患者中沒有觀察到這種關系。此外,LUAD患者中CXCL13的高表達與更好的無病生存率和總生存率相關,但在LUSC患者中沒有這種相關性。總之,研究發現B細胞反應在LUAD患者中具有重要作用,可能影響預后。
研究發現,TLS和B細胞反應在LUAD中可能具有保護作用,總腫瘤突變負擔與LUAD患者腫瘤區域內BCR庫多樣性和IgG頻率顯著相關。研究者檢查了非突變的腫瘤相關抗原,關注ERV包膜糖蛋白。結果表明,ERVK-7在LUAD患者中表達顯著上調,與LUSC患者相比更明顯。研究發現ERVK-7表達與CD8+ T細胞、NK細胞的轉錄特征及IgG頻率相關。45%的LUAD患者和0%的LUSC患者檢測到與HERV-K(HML-2)包膜蛋白反應的抗體。研究表明,ERVK-7轉錄增加可能由染色體1q22擴增誘導,從而導致HERV-K(HML-2)包膜反應抗體在大量LUAD患者中出現。

研究發現,腫瘤特異性B細胞克隆擴張與淋巴結相關。HERV-K(HML-2)包膜反應性抗體在LUAD中占據了抗腫瘤反應的很大比例,并產生強大的抗腫瘤效果。ICB治療后,這些抗體水平顯著上升,可能與抗腫瘤免疫有關。
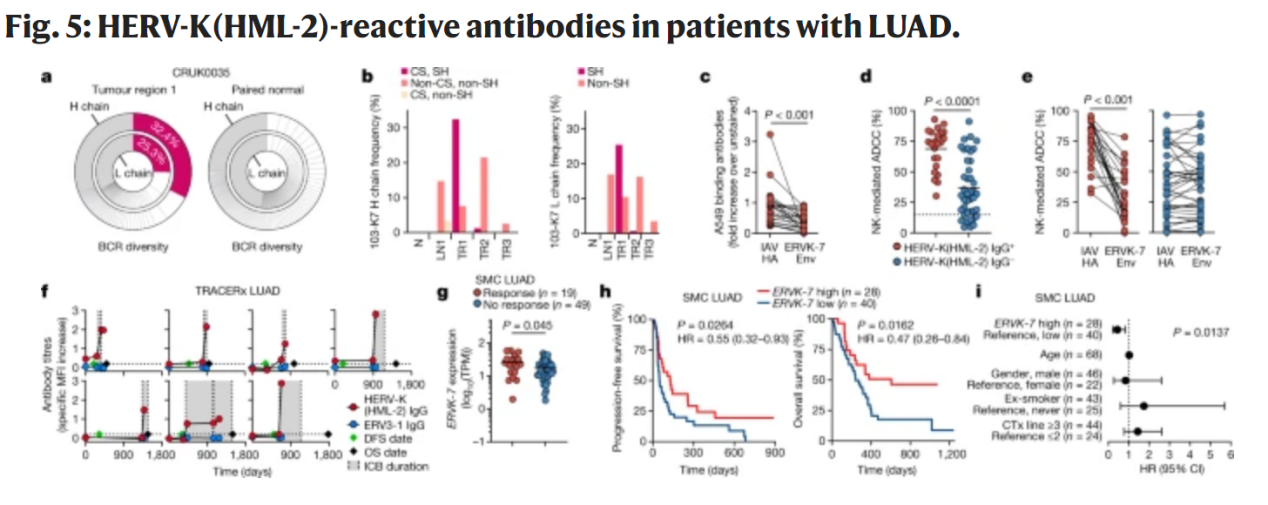
綜上所述,這篇文獻通過研究肺癌患者和小鼠模型中的B細胞反應,揭示了肺癌免疫治療中TLS的重要作用,并發現針對ERV的抗體有潛力成為有效的免疫治療靶標。
原文鏈接:https://www.nature.com/articles/s41586-023-05771-9
在抗體結合和親和力檢測實驗中,作者用到了武漢華美生物的重組ERV-K7包膜蛋白(CSB-CF351062HU)
Recombinant Human Endogenous retrovirus group K member 7 Env polyprotein
來源:in vitro E.coli expression system
蛋白長度:Full Length
表達區域:1-588aa
蛋白標簽:N-terminal 10xHis-tagged
肺癌是全球最常見的癌癥之一,也是最常導致死亡的癌癥。近年來,免疫治療已經成為肺癌治療的一個重要手段。弗朗西斯·克里克研究所(The Francis Crick Institute)Julian Downward和George Kassiotis等人于2023年4月發表在Nature上的一篇文章,探討了肺腺癌患者和小鼠肺腺癌引起的局部生發中心反應和腫瘤結合抗體,并進一步確定內源性逆轉錄病毒(ERV)包膜糖蛋白是主要的抗腫瘤抗體靶點。

B cell responses in a new LUAD model
為了研究B細胞和TLS在腫瘤進展和治療反應中的作用。研究者使用了一個新建立的LUAD模型,該模型基于KPAR細胞。研究發現KPAR腫瘤能夠刺激TLS形成和生發中心反應,而KPB6腫瘤則不能。此外,KPAR受試小鼠的血清中含有與KPAR結合的抗體,具有抗腫瘤活性。將KPAR受試小鼠的血清轉移到第二批KPAR受試小鼠中,可以顯著延長受試小鼠的生存期。這些抗腫瘤活性與腫瘤浸潤的自然殺傷(NK)細胞數量的顯著增加有關。總之,這些結果表明KPAR腫瘤能誘導招募和激活B細胞,并產生具有強大抗腫瘤活性的抗體。

Anti-tumour antibodies target an ERV
研究人員通過實驗探究KPAR模型中抗腫瘤抗體特異性的過程,發現抗腫瘤抗體在KPAR模型中主要靶向一類異常表達的內源性逆轉錄病毒(ERV),這可能為腫瘤免疫治療提供了新的靶點。在KPAR腫瘤模型中,研究人員發現了一種具有感染性的KPAR相關逆轉錄病毒(KARV),并證明其是主要的抗體靶點。通過使用83A25治療,研究人員觀察到野生型小鼠對KPAR挑戰的生存期顯著延長,同時在缺乏eMLV包膜糖蛋白免疫耐受的Emv2缺陷小鼠中,KPAR腫瘤生長受到延遲。這些發現揭示了異常表達的ERV作為自發產生的針對KPAR腫瘤的保護性抗腫瘤抗體的主要靶點,為未來腫瘤免疫治療研究提供了新的方向。

PD-L1 blockade boosts anti-ERV response
在本文中,研究者還探討了抗腫瘤抗體和GC反應是否對PD-1或PD-L1阻斷的治療效果有貢獻。實驗發現,PD-L1阻斷顯著延長了KPAR腫瘤小鼠的生存期,并擴大了局部GC B細胞和TFH細胞反應。PD-L1阻斷還顯著提高了腫瘤結合IgG和IgA抗體的滴度。此外,來自PD-L1阻斷治療小鼠的血清中,IgG和IgA抗體對KARV(KPAR相關逆轉錄病毒)感染的M. dunni細胞的結合增加,說明抗ERV抗體對KPAR腫瘤排斥的未處理和ICB治療有貢獻。總之,這些數據表明,抗PD-L1治療增強了對特定ERV抗原的抗體反應,并提高了抗腫瘤抗體的功能,從而改善了腫瘤治療效果。
B cell responses in targeted therapies
為了探討抗腫瘤B細胞反應是否對除ICB外的其他治療方法產生治療效果。研究者使用了靶向治療方法,包括高度選擇性的KRAS(G12C)抑制劑(G12Ci)。研究表明,針對性治療KRAS(G12C)抑制劑G12Ci可促進抗腫瘤B細胞反應,而全身性抑制MEK會阻礙這些反應。在G12Ci治療的小鼠模型中,B細胞可能對持久抗腫瘤反應和免疫記憶有積極作用。這些發現有助于了解B細胞在腫瘤治療中的作用,并指導未來的免疫治療策略。


CXCL13 therapy synergizes with ICB
B cell responses in patients with LUAD
ERV-reactive antibodies in patients with LUAD

ICB boosts human anti-ERV antibodies

綜上所述,這篇文獻通過研究肺癌患者和小鼠模型中的B細胞反應,揭示了肺癌免疫治療中TLS的重要作用,并發現針對ERV的抗體有潛力成為有效的免疫治療靶標。
原文鏈接:https://www.nature.com/articles/s41586-023-05771-9
在抗體結合和親和力檢測實驗中,作者用到了武漢華美生物的重組ERV-K7包膜蛋白(CSB-CF351062HU)
Recombinant Human Endogenous retrovirus group K member 7 Env polyprotein
來源:in vitro E.coli expression system
蛋白長度:Full Length
表達區域:1-588aa
蛋白標簽:N-terminal 10xHis-tagged











